La nefritis lúpica. Un reto terapéutico
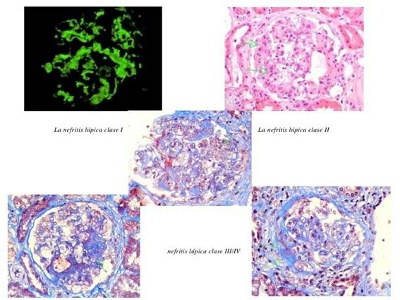
El lupus eritematoso generalizado (LEG), es un síndrome poligénico y multifactorial, caracterizado por alteraciones profundas y diversas de inmunorregulación, pérdida de la tolerancia y producción de autoanticuerpos patogénicos que se expresa con afección multiorgánica; la nefritis (NL) es frecuente y causa elevada morbimortalidad.
En el LEG hay un incremento en la apoptosis, como consecuencia de disregulación génica, alteraciones en el manejo y depuración de la cromatina y nucleosomas, conformación de autoanticuerpos y disfunción de células inmunes (presentadoras de antígeno, macrófagos, células T y B). Lo anterior se traduce en una infiltración tisular de células inmunes, incremento de citocinas (interferón, interleucina 17, 6 y factor de necrosis tisular, entre otras), y producción de autoanticuerpos como anti-ADN que se asocian a disfunción endotelial, de otras células y tejidos, como el renal.
La NL se acompaña de la modificación funcional y estructural de los podocitos y sus proteínas, que participan en el daño tisular.
El ADN nucleosomal y de complejos inmunes activan receptores TLR9 en células B, dendríticas y plasmacitoides. El estimulador de linfocitos B (BLyS o factor activador BAFF), el ligando que induce proliferación(APRIL) y el inductor débil de apoptosis de la familia de TNF (TWEAK) son citocinas que participan en el proceso inflamatorio y de autoinmunidad. Infecciones virales, productos bacterianos y medicamentos (algunos que disminuyen la metilación de ADN) estimulan células intrarrenales inmunes, hechos que conllevan proteinuria. La luz ultravioleta induce apoptosis de queratinocitos, aumenta la carga de células muertas en la ya ineficiente depuración de éstas y exacerba el LEG. Los complejos inmunes se relacionan a tipo, duración y gravedad de la NL, con depósitos mesangiales, subendoteliales o subepiteliales, y concurrente activación del complemento. Los complejos inmunes se unen a receptores (Fc, TLR y complemento), activan células renales (macrófagos, células dendríticas, podocitos), atraen leucocitos (a través de moléculas de adhesión y proteínas de complemento), incrementan la expresión y producción de citocinas (la IL-17 induce células T nefrocitopáticas CD3+/CD4+ o CD3+ CD4-/8−), activan al endotelio, condicionan proliferación extracapilar (formación de medias lunas), inflamación periglomerular y esclerosis1.
Uno de los retos en el LEG lo representa el tratamiento de la NL. Los esteroides inicialmente considerados como piedra angular, por sí mismos no han sido lo suficientemente eficaces para alcanzar remisión completa y preservar la función renal. Aunque con terapia combinada con ciclofosfamida (CFM) se alcanzan mejores resultados, la remisión sostenida es < 40%, con pérdida de la función renal en > 40% de aquellos con NL tipo iv, lo que enfatiza la necesidad de otras modalidades terapéuticas; además, las recaídas son frecuentes, del 27 al 66%, particularmente ante terapia inadecuada y respuesta parcial, pero menores con micofenolato de mofetilo (MMF). Las recaídas pueden ser nefríticas o proteinúricas, asociadas a diversos biomarcadores que sobrepasan a los clásicos incrementos de ADN de doble cadena (dsDNA) e hipocomplementemia; incluyen la proteína quimioatrayente de monocitos (MCP-1), quimiocinas, lipocalina asociada a gelatinasa del neutrófilo (NGAL) y TWEAK urinario, entre otros. Aceptamos como factores de riesgo asociados a recaídas, la edad < 30 años, el género masculino, la raza afroamericana, el retraso en la iniciación de tratamiento, el tiempo prolongado para alcanzar remisión, la persistencia de hipocomplementemia a pesar de respuesta, la ausencia de respuesta completa, el puntaje alto de actividad del LEG, la hipertensión, la afección neurológica y las dosis bajas de inmunosupresores, además de la presencia de microangiopatía y de proliferación extracapilar.
La EULAR, en conjunto con las Asociaciones Renal Europea y de Trasplantes y Diálisis, sugiere realizar biopsia ante cualquier indicio de afección renal, clasificar la histología, con el objetivo terapéutico de alcanzar respuesta completa (relación proteinuria creatinuria < 50 mg/mmol o proteinuria < 0,5 g/d; tasa de filtración glomerular [TFG] normal o casi normal: < 10% menor de lo normal en anormalidad previa) o respuesta parcial (> 50% reducción de proteinuria y TFG normal o casi normal).
Abud-Mendoza C. Nefritis lúpica: ¿avances en el conocimiento de su inmunopatogénesis sin los esperables logros terapéuticos? Reumatol Clin. 2013;9:77–9.
David Cimbaluk Pathology, classification and pathogenesis of lupus glomerulonephritis. Diagnostic Histopathology, Volume 19, Issue 5, 2013, pp. 151-157
Dra Ana Mª Oltra
Coordinadora Blog Renal
Nefrología. CHGUV








Comentarios recientes